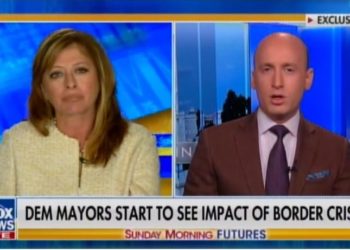
US Notfallzulassung von Pfizer und BioNTech mit dicken Warnhinweisen.
Pfizer Inc. und BioNTech SE haben heute einen Antrag auf Notfallzulassung (Emergency Use Authorization, „EUA”) für eine 10-µg Auffrischungsimpfung des Pfizer-BioNTech COVID-19 bei Kindern im Alter von 5 bis 11 Jahren (auch bekannt als Kinder im Alter von 5 bis unter 12 Jahren) bei der U.S. Arzneimittelbehörde (Food and Drug Administration, „FDA”) eingereicht.
Der Antrag beinhaltet Daten einer Phase 2/3 Studie mit Kindern im Alter von 5 bis 11 Jahren ungefähr 6 Monate, die nach der zweiten Dosis der primären Impfserie mit dem Pfizer-BioNTech COVID-19-Impfstoff eine Auffrischungsimpfung erhielten. Die Notfallzulassung für die primäre Impfserie mit zwei Dosen à 10 µg wurde im Oktober 2021 erteilt.
Die Unternehmen planen außerdem, die Daten in den kommenden Wochen bei der Europäischen Arzneimittel-Agentur (European Medicines Agency, „EMA“) sowie weiteren Zulassungsbehörden weltweit einzureichen.
Im Pressebrief wird interessanterweise auch ausdrücklich folgend Hingewiesen:
Suchen Sie sofort einen Arzt auf, wenn Sie eines der folgenden Symptome nach Erhalt der Impfung haben:
-
- Brustschmerzen
- Kurzatmigkeit
- Das Gefühl eines schnell schlagenden, flatternden oder hämmernden Herzens
- Nach der Verabreichung von injizierbaren Impfstoffen, einschließlich Pfizer-BioNTech COVID-19 Impfstoff oder COMIRNATY® (COVID-19 Impfstoff, mRNA) können Ohnmachtsanfälle auftreten, bei denen Sie stürzen und sich verletzen können. Aus diesem Grund kann Ihr behandelnder Arzt Sie bitten, sich nach der Impfung 15 Minuten lang hinzusetzen oder hinzulegen.
- Bei manchen Menschen mit geschwächtem Immunsystem kann es zu einer verminderten Immunantwort auf den Impfstoff COVID-19 von Pfizer-BioNTech oder COMIRNATY® (COVID-19-Impfstoff, mRNA) kommen.
- Weitere Nebenwirkungen sind Schmerzen an der Injektionsstelle, Erschöpfung, Kopfschmerzen, Muskelschmerzen, Schüttelfrost, Gelenkschmerzen, Fieber, Schwellungen an der Injektionsstelle, Rötungen an der Injektionsstelle, Übelkeit, Unwohlsein, geschwollene Lymphknoten (Lymphadenopathie), verringerter Appetit, Durchfall, Erbrechen, Schmerzen im Arm und Ohnmacht in Verbindung mit der Verabreichung des Impfstoffs.
Diese Liste an möglichen Nebenwirkungen ist gegebenenfalls nicht vollständig. Kontaktieren Sie den Impfstoffhersteller oder Ihren behandelnden Arzt bezüglich belastender Nebenwirkungen oder Nebenwirkungen, die nicht abklingen.
-
- Bei unerwünschten Nebenwirkungen sollten Sie immer Ihren Arzt konsultieren. Melden Sie alle durch die Impfung ausgelösten Nebenwirkungen der US-amerikanischen FDA und dem Vaccine Adverse Event Reporting System (VAERS) der Centers for Disease Control and Prevention (CDC). Sie erreichen VAERS unter der gebührenfreien Nummer +1-800-822-7967 oder online über www.vaers.hhs.gov/reportevent.html. Sie können Nebenwirkungen auch bei Pfizer Inc. unter www.pfizersafetyreporting.com oder unter der Telefonnummer 1-800-438-1985 melden.
Dazu fügt es noch hinzu:
Personen sollten den Impfanbieter über ihren Gesundheitszustand informieren, einschließlich:
-
- einer zuvor aufgetretenen Myokarditis (Herzmuskelentzündung) oder Perikarditis (Herzbeutelentzündung)
- Fieber
- dem Vorliegen einer Blutgerinnungsstörung oder der Einnahme von Blutverdünnungsmittel
- dem Vorliegen einer Immunschwäche oder der Einnahme von immunschwächenden Medikamenten
- dem Vorliegen einer Schwangerschaft, dem Plan demnächst schwanger zu werden oder ob derzeit gestillt wird
Notfallzulassung
Notfallverwendungen des Produktes wurden nicht durch die FDA zugelassen oder lizensiert, sondern im Rahmen einer Notfallzulassung (Emergency Use Authorization, „EUA“) zur Prävention der Coronaviruserkrankung 2019 (COVID-19) bei Personen ab 12 Jahren bzw. bei Personen im Alter von 5 bis 11 Jahren unter den jeweils geltenden Bedingungen genehmigt. Die Notfallzulassungen im Rahmen der EUA sind nur für die Dauer der Erklärung zulässig, in der Umstände vorliegen, die die Genehmigung einer Notfallzulassung des Medizinproduktes gemäß Abschnitt 564(b)(1) des FD&C Act rechtfertigen, es sei denn, die Erklärung wird früher beendet oder die Genehmigung widerrufen.
Quelle: Biontech
Biontech Presse